Un estudio de investigadores del CONICET en la Fundación Instituto Leloir caracterizó el rol de dos nuevas proteínas de Brucella que, al detectar la presencia de hierro y manganeso en el interior de las células del organismo que invaden, “apagan” los genes que hasta ese momento le permitieron sobrevivir a las defensas naturales. Así, la bacteria optimiza el uso de su energía para consolidar su replicación. El hallazgo permite pensar en el potencial uso de estos “sensores” para el diseño de futuros tratamientos contra infecciones agudas.
(Agencia CyTA-Leloir).- Los estudios sobre bacterias que causan enfermedades se suelen centrar en entender cómo “encienden” su ataque para infectar a las células. Pero comprender cómo lo apagan a tiempo, para evitar gastar energía innecesaria o poner en alerta extrema al sistema inmune del organismo invadido, puede ser tan o más importante cuando lo que se busca es conseguir intervenciones que puedan evitar o frenar su avance.
El grupo del Laboratorio de Microbiología Molecular y Celular, que dirige Angeles Zorreguieta en la Fundación Instituto Leloir, reveló en Scientific Reports la identificación de dos proteínas –hasta ese momento sin caracterizar– de la bacteria Brucella y sugiere que éstas actúan como “sensores” de hierro y manganeso en el interior de la célula, un rol fundamental para consolidar el avance de la infección: cuando detectan la presencia de esos metales, envían la señal de “apagarse” a los genes que sintetizan otros tipos de proteínas llamadas factores de virulencia, que ayudan al patógeno a resistir la defensa celular.
De esa manera, la bacteria registra que ya está en un lugar seguro (el retículo endoplasmático), se pone en modo “ahorro de energía” y deja de producir los factores de virulencia para destinar sus mayores esfuerzos solamente a replicarse.

Gastón Amato (centro, camisa blanca), Angeles Zorreguieta (rojo) y Rodrigo Sieira (de anteojos), junto al resto de los miembros del Laboratorio de Microbiología Molecular y Celular de la FIL.
“La identificación de un nexo entre la regulación de homeostasis de metales y factores de virulencia dentro de las células del sistema inmune propone un mecanismo molecular de adaptación intracelular para esta bacteria”, resaltó a la Agencia CyTA-Leloir Rodrigo Sieira, investigador del CONICET y quien junto a Zorreguieta lideró el trabajo que tiene al becario doctoral Gastón Amato como primer autor. “Este mecanismo propuesto tiene potencial utilidad para el diseño de futuras estrategias para tratar infecciones agudas”, añadió Sieira.
La brucelosis es una enfermedad que se transmite de los animales a los seres humanos y es un problema de salud pública en la Argentina (provoca fiebre, dolor de cabeza, exceso de sudoración, fatiga, debilidad y falta de apetito, entre otros síntomas). Tiene un gran impacto económico porque infecta al ganado bovino, caprino y porcino, y si bien hay disponibles vacunas para prevenirla en vacas y en cabras, no existen para ser aplicadas en cerdos ni en personas. A nivel mundial, se reportan 500 mil casos anuales y se estima que 2.400 millones de personas están en riesgo de contraerla.
En acción
Para el estudio, el grupo de la FIL se propuso identificar las proteínas clave que controlan la expresión de los genes de virulencia de la bacteria. Para eso, primero utilizó herramientas de bioinformática para analizar regiones regulatorias de un grupo de genes que la bacteria activa cuando ingresa a una célula del sistema inmune. “Buscamos allí aquellas secuencias de ADN que se repiten y eso nos condujo a la identificación de secuencias similares a sitios de unión para factores de transcripción de la familia Fur”, explicó Sieira.
Los reguladores Fur son proteínas cuya función consiste en detectar metales. Cuando eso ocurre, se induce su unión al ADN y eso lleva al silenciamiento de los genes encargados de incorporar dichos metales. “Eso evita que éstos lleguen a concentraciones tóxicas para la bacteria”, aseguró el investigador.
Los científicos demostraron que Mur y Fur4, dos proteínas pertenecientes a la familia Fur, apagan la expresión de genes esenciales para la virulencia de Brucella en respuesta al agregado de hierro o manganeso en bacterias cultivadas en laboratorio. “Vimos que Mur y Fur4 los apagan una vez que ya no son necesarios, luego de que la bacteria evitó la degradación de los lisosomas y empezó a replicarse en la célula hospedadora”, describió Sieira. En cambio, en cepas modificadas de Brucella, que carecen de Mur y Fur4, los genes de virulencia no se apagan y siguen activos, incluso por más tiempo.
“Nuestros experimentos sugieren que las proteínas Mur y Fur4 detectan fluctuaciones en la disponibilidad de metales durante la transición desde un ambiente hostil, ácido y carente de nutrientes, hacia condiciones favorables para la replicación”, resaltó Sieira. De este modo Brucella reprime la expresión de genes específicos una vez que ya cumplieron su función, y de esa manera evita un gasto energético innecesario en su síntesis y ensamblado.
A partir de la comprensión de que a través de los reguladores Fur4 y Mur esta bacteria usaría señales del entorno –la presencia de hierro y manganeso– para decidir cuándo encender y cuando apagar sus genes de virulencia, los científicos le habrían encontrado una debilidad. El desafío, ahora, será ver si se pueden idear tratamientos que engañen a esos sensores para que apaguen genes antes de tiempo o para que nunca los enciendan, dándole una ventaja crucial a las células de defensa del sistema inmune del paciente.
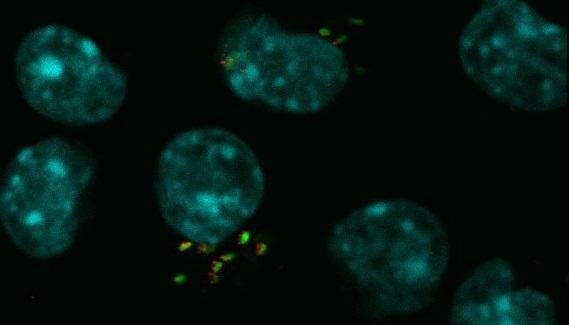
Imagen de microscopía de fluorescencia donde se ve a Brucella infectando una célula de ratón: en rojo y verde, la bacteria; en cyan, el ADN del núcleo celular.